La Energía Involucrada en los Cambios de Estado: Todo lo que Necesitas Saber
Introducción a los Cambios de Estado
¿Alguna vez te has preguntado qué sucede cuando el hielo se convierte en agua o cuando el agua se evapora y se convierte en vapor? Estos fenómenos, aunque cotidianos, son ejemplos fascinantes de cambios de estado, donde la energía juega un papel fundamental. La energía involucrada en estos cambios es crucial para entender no solo la química detrás de ellos, sino también cómo afectan nuestra vida diaria. En este artículo, vamos a explorar a fondo qué son los cambios de estado, la energía que los acompaña y cómo se manifiestan en nuestro entorno.
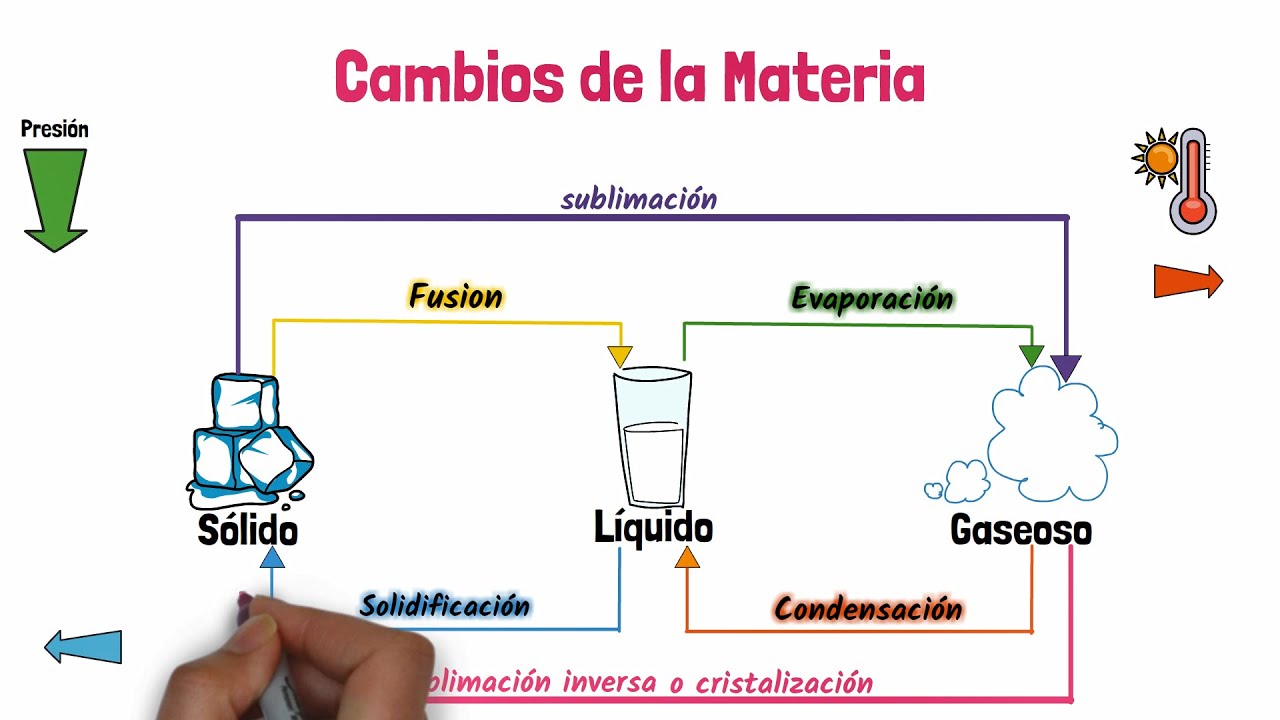
Los cambios de estado se producen cuando una sustancia pasa de una forma física a otra, como de sólido a líquido o de líquido a gas. Pero, ¿qué es lo que provoca estos cambios? La respuesta está en la energía. La energía térmica, que es el calor, es la clave que permite que las partículas de una sustancia se muevan más rápido o más lento, cambiando así su estado. A medida que la energía térmica se incrementa, las moléculas se separan más, pasando de un estado sólido, donde están muy unidas, a un estado líquido, y finalmente a un estado gaseoso, donde están casi libres. Ahora, adentrémonos en los diferentes tipos de cambios de estado y cómo la energía se manifiesta en cada uno de ellos.
Tipos de Cambios de Estado
Fusión: De Sólido a Líquido
La fusión es el primer cambio de estado que vamos a explorar. Imagina que tienes un cubo de hielo en tu mano. A medida que lo sostienes, tu calor corporal le transfiere energía térmica. Este calor hace que las moléculas de hielo comiencen a moverse más rápidamente, rompiendo las fuerzas que las mantienen unidas en una estructura sólida. Cuando el hielo alcanza su punto de fusión, se convierte en agua. Este proceso no solo es interesante desde un punto de vista físico, sino que también tiene implicaciones en la vida cotidiana, desde la forma en que hacemos cubitos de hielo hasta cómo funcionan los glaciares en el clima global.
¿Sabías que durante la fusión, la temperatura del hielo se mantiene constante a 0 °C hasta que se haya derretido por completo? Esto se debe a que la energía que se está utilizando no está aumentando la temperatura, sino que se está utilizando para romper las uniones entre las moléculas. Este fenómeno es un gran ejemplo de cómo la energía puede actuar de manera sorprendente, y es fundamental en procesos como la fabricación de alimentos y la refrigeración.
Vaporización: De Líquido a Gas
Pasemos ahora a la vaporización, el proceso en el que un líquido se convierte en gas. Todos hemos visto esto en acción cuando hervimos agua. Al calentar agua en una olla, la energía térmica se transfiere a las moléculas de agua, haciendo que se muevan más rápido. Una vez que el agua alcanza su punto de ebullición, comienza a transformarse en vapor.
Lo interesante aquí es que la vaporización puede ocurrir de dos maneras: por ebullición o por evaporación. La ebullición es lo que sucede cuando el líquido alcanza una temperatura específica y burbujas de vapor se forman en todo el líquido. Por otro lado, la evaporación puede ocurrir a cualquier temperatura, siempre que las moléculas de la superficie del líquido tengan suficiente energía para escapar. Este proceso es vital en la naturaleza, ya que es una de las formas en que el agua se recicla en el medio ambiente.
Condensación: De Gas a Líquido
La condensación es el proceso inverso a la vaporización. ¿Alguna vez has notado cómo el vapor de agua se convierte en gotas de agua en la tapa de una olla después de hervir? Esto es condensación en acción. Cuando el vapor se enfría, pierde energía térmica y las moléculas se agrupan nuevamente, formando líquido. Este proceso es esencial para la formación de nubes y la lluvia, lo que a su vez es crucial para el ciclo del agua en nuestro planeta.
Una analogía que puede ayudar a visualizar esto es pensar en una fiesta. Imagina que todos están bailando (representando a las moléculas en un estado gaseoso). Cuando la música se detiene (representando la pérdida de energía), la gente se agrupa y se sienta (representando la formación de líquido). Así es como las moléculas de gas se agrupan para formar un líquido durante la condensación.
Solidificación: De Líquido a Sólido
La solidificación es el último de los cambios de estado que vamos a discutir. Este es el proceso en el que un líquido se convierte en sólido, como cuando el agua se congela en hielo. A medida que se elimina la energía térmica del agua, las moléculas comienzan a moverse más lentamente y se agrupan en una estructura ordenada, formando un sólido.
Un ejemplo cotidiano de solidificación es el proceso de hacer helado. Cuando la mezcla de helado se enfría, las moléculas de agua en la mezcla pierden energía y se convierten en cristales de hielo. Este proceso no solo es fascinante desde un punto de vista científico, sino que también es un gran recordatorio de cómo la energía afecta nuestra vida diaria, desde la cocina hasta el clima.
La Energía y los Cambios de Estado
Calor Latente: La Energía Oculta
Una de las ideas más importantes relacionadas con los cambios de estado es el concepto de calor latente. Este es el calor que se absorbe o se libera durante un cambio de estado, sin que haya un cambio en la temperatura. Por ejemplo, cuando el hielo se derrite, absorbe calor, pero su temperatura no cambia hasta que todo el hielo se ha convertido en agua. Este calor latente es crucial en muchos procesos naturales y artificiales.
Imagina que estás cocinando. Cuando agregas agua a una olla caliente, al principio no ves que la temperatura suba inmediatamente. Eso es porque el agua está absorbiendo calor latente para comenzar a hervir. Este concepto es fundamental en la meteorología, la refrigeración y la ingeniería, ya que influye en cómo entendemos y controlamos los procesos térmicos.
Impacto en el Medio Ambiente
Los cambios de estado también tienen un gran impacto en nuestro medio ambiente. Por ejemplo, la evaporación del agua de los océanos es un factor clave en el ciclo del agua, que es esencial para la vida en la Tierra. Sin la energía del sol que permite que el agua se evapore, no tendríamos lluvia, ríos o lagos.
Además, los cambios de estado están relacionados con el clima. El calentamiento global, que está provocando un aumento en las temperaturas, también está afectando los patrones de evaporación y condensación. Esto puede llevar a fenómenos climáticos extremos, como sequías o tormentas intensas. Es crucial que entendamos cómo la energía y los cambios de estado están interrelacionados para abordar estos desafíos ambientales.
Preguntas Frecuentes
1. ¿Qué es el calor latente?
El calor latente es la energía que se absorbe o se libera durante un cambio de estado sin que haya un cambio en la temperatura. Es fundamental en procesos como la fusión y la vaporización.
2. ¿Por qué el hielo no se calienta hasta que se derrite?
El hielo no se calienta porque la energía que se le está proporcionando se utiliza para romper las uniones entre las moléculas, en lugar de aumentar su temperatura.
3. ¿Cómo afectan los cambios de estado al clima?
Los cambios de estado, como la evaporación y la condensación, son fundamentales en el ciclo del agua y afectan los patrones climáticos. El calentamiento global está alterando estos procesos, lo que puede llevar a fenómenos climáticos extremos.
4. ¿Cuál es la diferencia entre ebullición y evaporación?
La ebullición es un tipo de vaporización que ocurre a una temperatura específica, mientras que la evaporación puede ocurrir a cualquier temperatura, siempre que las moléculas en la superficie tengan suficiente energía para escapar.
5. ¿Por qué es importante entender los cambios de estado?
Entender los cambios de estado es crucial para diversas aplicaciones, desde la meteorología hasta la ingeniería y la cocina. Nos ayuda a comprender mejor el mundo que nos rodea y a abordar desafíos ambientales.
Este artículo explora los cambios de estado y la energía involucrada en ellos de una manera accesible y comprensible. ¡Espero que te haya gustado!